 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


计算25℃,c(HCl)=10mol·L-1的盐酸中,当其他物种均为标准状态时,反应MnO2+2Cl-+4H+=Mn2++Cl2+2H2O的自发方向
计算25℃,c(HCl)=10mol·L-1的盐酸中,当其他物种均为标准状态时,反应MnO2+2Cl-+4H+=Mn2++Cl2+2H2O的自发方向及反应的标准平衡常数。已知Φ(MnO2/Mn2+)=1.22V,Φ(Cl2/Cl-)=1.36V
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


计算25℃,c(HCl)=10mol·L-1的盐酸中,当其他物种均为标准状态时,反应MnO2+2Cl-+4H+=Mn2++Cl2+2H2O的自发方向及反应的标准平衡常数。已知Φ(MnO2/Mn2+)=1.22V,Φ(Cl2/Cl-)=1.36V
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“计算25℃,c(HCl)=10mol·L-1的盐酸中,当其他…”相关的问题
更多“计算25℃,c(HCl)=10mol·L-1的盐酸中,当其他…”相关的问题
第1题
计算反应=Hg2++Hg在25℃时的标准平衡常数,以及在
水溶液中,c(
)与c(
)之比。标准状态下,
是否易于歧化?在一含有HgS和Hg2S沉淀的溶液中,c(
)与c(
)之比又为多少?二沉淀能否大量共存?写出有关反应式,并判断向
溶液中通入H2S,将生成何产物。试分析
在何条件下易于歧化?已知
=0.920V,
,
(HgS)=4×10-53,
(Hg2S)=1×10-45
第3题
能使含Sn2+、Fe2+、Cl-、Br-混合液中的Sn2+、Fe2+氧化成Sn4+、Fe3+,而Cl-、Br-不被氧化的氧化剂为:已知:φθ(Sn4+/Sn2+)=0.154V,φθ(Fe3+/Fe2+)=0.771V,φθ(Cl2/Cl-)=1.36V,φθ(Br2/Br-)=1.07V; φθ(Ag+/Ag)=0.799V,φθ(Cu2+/Cu)=0.337V,φθ(I2/I-)=0.54V
A.K2Cr2O7 B.AgNO3 C.CuSO4 D.I2
第4题
已知,则
(Cu2+/Cul),
(Cu2+/CuBr),
(Cu2+/CuCl)由低到高的顺序为:
A.
B.
C.
D.
第5题
下列叙述不正确的为:
A.有H+或OH-参加反应的电极,电极电势肯定与介质酸度有关;
B.无H+或OH-参加反应的电极,电极电势肯定与介质酸度无关;
C.任意温度下,标准氢电极的电极电势均等于0;
D.电极![]() /Fe2+的电极电势与酸度有关。
/Fe2+的电极电势与酸度有关。
第6题
下列电极的电极电势与介质酸度无关的为:
A.![]() ; B.
; B.![]() /ClO-; C.ClO-/Cl2;D.Cl2/Cl-。
/ClO-; C.ClO-/Cl2;D.Cl2/Cl-。
第7题
Fe(II)在碱性介质中比在酸性介质中更易被空气氧化,原因为:
A.碱性介质中,氧气氧化性增强;
B.酸性介质中,氧气氧化性减弱。;
C.Fe(OH)3的溶度积远小于Fe(OH)2的溶度积;
D.碱性介质中,氧气氧化性减弱。
第8题
已知,![]() (Cu2+/Cu)=0.34V,
(Cu2+/Cu)=0.34V,![]() (Cu+/Cu)=0.52V,则
(Cu+/Cu)=0.52V,则![]() (Cu2+/Cu+)等于:
(Cu2+/Cu+)等于:
A.0.16V; B.0.18V; C.0.36V;D.0.43V。
第9题
298.15K,原电池2Fe2++Cl2=2Fe3++2Cl-电动势为0.60V,其中Cl2和Cl-均处于标准状态。已知3+(Fe3+/Fe2+)=0.77V,(Cl2/Cl-)=1.36V。此原电池中,c(Fe3+)/c(Fe2+)等于:
A.0.68; B.0.98; C.0.52;D.1.53。
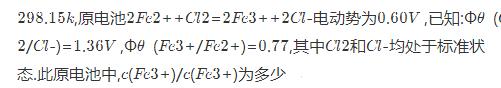
第10题
标准状态下,水溶液中不能共存的一组物质为:
A.![]() ,Cl-; B.
,Cl-; B.![]() ,Cl-; C.
,Cl-; C.![]() ,Fe3+;D.Fe3+,Sn2+。
,Fe3+;D.Fe3+,Sn2+。


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧