 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
分别判断在标准状态下,下列两个歧化反应能否发生?
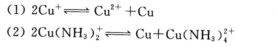
请帮忙给出正确答案和分析,谢谢!
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“分别判断在标准状态下,下列两个歧化反应能否发生?”相关的问题
更多“分别判断在标准状态下,下列两个歧化反应能否发生?”相关的问题
第1题
将20 cm30.025 mol.dm-3的AgNO3溶液与2.0 cm31.0mol.dm-3的氨溶液混合,所得溶液中Ag(NH3)2+浓度是多少?在此溶液中再加入2.0 cm31.0mol.dm-3的KCN,求所得溶液中Ag(NH3)2+浓度是多少(忽略CN-水解)?配位反应的方向与配合物稳定性关系如何?
请帮忙给出正确答案和分析,谢谢!
第2题
某溶液中原来Fe3+和Fe2+的浓度相等,若向溶液中加入KCN固体,最终使CN-离子浓度为1.0 mol.dm-3,计算这时电极反应
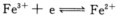 的电极电势是多少。
的电极电势是多少。
请帮忙给出正确答案和分析,谢谢!
第3题
电极反应Au3++3e
 Au的标准电极电势为1.52 V,若向溶液中加入足够的Cr以形成AuCl4-,当Cl-和AuCl4-的浓度均为1.00 mol.dm-3时,电极电势降为1.00 V。试计算反应Au3++4Cl-
Au的标准电极电势为1.52 V,若向溶液中加入足够的Cr以形成AuCl4-,当Cl-和AuCl4-的浓度均为1.00 mol.dm-3时,电极电势降为1.00 V。试计算反应Au3++4Cl-
 AuCl4-的配位平衡常数(K稳)。
AuCl4-的配位平衡常数(K稳)。
请帮忙给出正确答案和分析,谢谢!
第4题
分别计算Zn(OH)2溶于氨水生成Zn(OH)42-和Zn(NH3)42+时的平衡常数K。 若控制[NH3.H2O]=[NH4+]=0.10 mol.dm-3,则Zn(OH)2溶于NH3.H2O中主要生成哪一种配离子?Zn(NH3)42+和Zn(OH)42-浓度比值是多少?
请帮忙给出正确答案和分析,谢谢!


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧