题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
有电池Hg(l)|硝酸亚汞(m1),HNO3(m)||硝酸亚汞(m2),HNO3(m)|Hg(l),电池中HNO3的浓度均为m=0.1mol·kg-1。在291
有电池Hg(l)|硝酸亚汞(m1),HNO3(m)||硝酸亚汞(m2),HNO3(m)|Hg(l),电池中HNO3的浓度均为m=0.1mol·kg-1。在291K时,维持m2/m1=10的情形下,Ogg(奥格)对该电池进行了一系列测定,求得电动势的平均值为0.029V。试根据这些数据确定亚汞离子在溶液中是以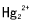 还是Hg+形式存在。
还是Hg+形式存在。
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案