 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
若要配制pH=8.54的NH4+—NH3缓冲溶液时,已知NH4+的解离常数为5.6×10-10,pKa为9.24,则NH4+与NH3的物质的量浓度之比为()
A.2.0
B.0.2
C.1.0
D.5
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.2.0
B.0.2
C.1.0
D.5
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“若要配制pH=8.54的NH4+—NH3缓冲溶液时,已知NH…”相关的问题
更多“若要配制pH=8.54的NH4+—NH3缓冲溶液时,已知NH…”相关的问题
第1题
A.2.0
B.0.2
C.1.0
D.5.0
第4题
计算0.20mol/L NH4CN溶液的pH值。 [Ka(HCN)=7.2×10-10,Ka(NH4+)=5.6×10-10]
第6题
根据已知数据,选择下列物质配制缓冲溶液,如欲配制pH=5.00的缓冲溶液,自行设计并说明应如何配制。
HF HAc NH+4HCN HS-
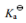 =3.5×10-4
=3.5×10-4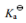 =1.8×10-5
=1.8×10-5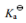 =5.6×10-10
=5.6×10-10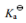 =4.93×10-10
=4.93×10-10 =1.1×10-12
=1.1×10-12
第7题
A.pH = 7
B.pH = 14
C.pH = pKb
D.pH = 14 - pKb
E.pH = 14 + pKb
第9题
在pH=10.0的氨性缓冲溶液中,若c(NH4+)+c(NH3)=1.0mol·dm-3,计算Zn2+离子的配合效应系数αM及Zn2+与EDTA的配合物条件稳定常数K'ZnY。
(已知:NH3·H2O的Kb=1.8×10-5;pH=10.0时,lgαY(H)=0.45;锌氨配合物的各级累积稳定常数为β1=102.27,β2=104.61,β3=107.01,β4=109.06,lgK(ZnY)=16.50)


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧