题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已 知 298 K 时,Sn (s) + Cl2 (g) → SnCl2 (s) 的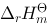 (1) = -349.8 kJ·mol-1, SnCl2 (s) + Cl2 (g) → SnCl4 (l) 的
(1) = -349.8 kJ·mol-1, SnCl2 (s) + Cl2 (g) → SnCl4 (l) 的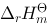 (2) = -195.4 kJ·mol-1, 则
(2) = -195.4 kJ·mol-1, 则 Sn (s) + Cl2 (g) →
Sn (s) + Cl2 (g) → SnCl4 (l) 的
SnCl4 (l) 的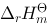 为
为
A.-545.2 kJ·mol-1
B.-272.6 kJ·mol-1
C.154.4 kJ·mol-1
D.-154.4 kJ·mol-1
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案


 的
的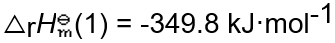 ,
,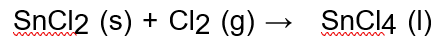 的
的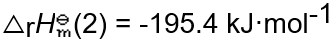 ,则
,则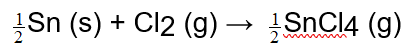 的
的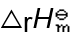 为................()。
为................()。
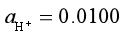 ,O2在阳极上析出的超电势为0.50 V,E?(H2O, H+?O2(g)?Pt)= 1.23 V。常数R = 8.314 J×mol-1×K-1,F = 9.65 ′ 104 C?mol-1。298 K时分解电压等于()V。精确保留至小数点后2位。
,O2在阳极上析出的超电势为0.50 V,E?(H2O, H+?O2(g)?Pt)= 1.23 V。常数R = 8.314 J×mol-1×K-1,F = 9.65 ′ 104 C?mol-1。298 K时分解电压等于()V。精确保留至小数点后2位。