 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
已知电极反应Hg2Cl2+2e→2Hg+2Cl-则25℃时其电极电位为()
A.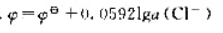
B.
C.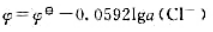
D.
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.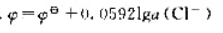
B.
C.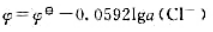
D.
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“已知电极反应Hg2Cl2+2e→2Hg+2Cl-则25℃时其…”相关的问题
更多“已知电极反应Hg2Cl2+2e→2Hg+2Cl-则25℃时其…”相关的问题
第1题
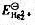 和Hg2Cl2的Kap ,计算
和Hg2Cl2的Kap ,计算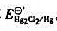 如溶液中Cl-浓度为0.010mol·L-1,Hg2Cl2/Hg电对的电势为多少?
如溶液中Cl-浓度为0.010mol·L-1,Hg2Cl2/Hg电对的电势为多少?
第3题
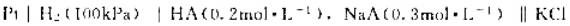 (饱和)|Hg2Cl2|Hg的电动势为0.762V,
(饱和)|Hg2Cl2|Hg的电动势为0.762V,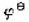 =0.244V,求HA的解离常数(忽略液接电位及离子强度)。
=0.244V,求HA的解离常数(忽略液接电位及离子强度)。
第4题
(1)H++Zn→Zn2++H2
(2)Fe3++Hg+Cl-→Hg2Cl2+Fe2+
(3)Pb2++SO2-4→PbSO4
(4)Ag++2NH3→[Ag(NH3)2]+
第5题
(1)H++Zn→Zn2++H2
(2)Fe3++Hg+Cl-→Hg2Cl2+Fe2+
(3)Pb2++SO2-4→PbSO4
(4)Ag++2NH3→[Ag(NH3)2]+
第6题
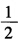 Hg2Cl2(s)→Agcl(s)+Hg(l) 已知298K时,此电池反应的焓变△rHm为5435J/mol,各物质的规定熵数据为 物质 Ag(s) AgCl(s) Hg(1) Hg2Cl2(s) SmΘ/(J/K.mol) 42.7 96.2 77.4 195.6 试计算该温度下电池的电动势E及电池电动势的温度系数
Hg2Cl2(s)→Agcl(s)+Hg(l) 已知298K时,此电池反应的焓变△rHm为5435J/mol,各物质的规定熵数据为 物质 Ag(s) AgCl(s) Hg(1) Hg2Cl2(s) SmΘ/(J/K.mol) 42.7 96.2 77.4 195.6 试计算该温度下电池的电动势E及电池电动势的温度系数
 。
。
第7题
A、电极反应为Hg22++2e→2Hg
B、属于第一类电极
C、对阴离子可逆,电极电势较稳定
D、电极电势为φ(Hg2Cl2)=φθ(Hg2Cl2)+(RT/2F)lna(Cl-)


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧