题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
反应N2O5+NO→3NO2在25℃时进行.第一次实验:pi(N2O5)=1.0X102Pa
反应N2O5+NO→3NO2在25℃时进行.第一次实验:
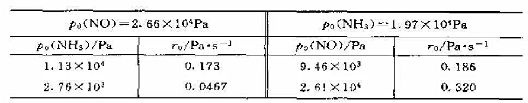
pi(N2O5)=1.0X102Pa,pi(NO)=1.0X104Pa(pi表示初始分压力),以Inp(N2O5)对t作图得一直线,由图还求得N2O5的半;衰期为2h;第二次实验:pi(N2O5)=pi(NO)=5.0X103Pa,并测得下列数据:
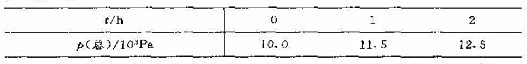
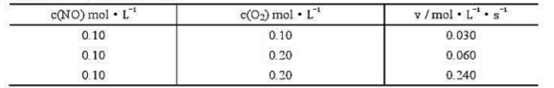
(1)设实验的速率公式形式为r=k[p(N2O5)]α[p(NO)]β.试求α、β值,并求算反应的表观速率常数k值;
(2)设该反应的机理为:
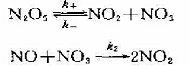
试推断在怎祥的条件下,由该机理导出的速率公式能够与实验结果一致?
(3)当pi(N2O5)=1.00X104Pa,pi(NO)=1.0X102Pa,NO反应掉一半器要多少时间?
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案