 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
恒容反应2NO2→2NO+O2试写出NO2的消耗迷率,NO和O2的生成速串,以及它们和反应速率的关系.
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“恒容反应2NO2→2NO+O2试写出NO2的消耗迷率,NO和…”相关的问题
更多“恒容反应2NO2→2NO+O2试写出NO2的消耗迷率,NO和…”相关的问题
第1题
对于反应2NO(g)+O2(g)====2NO2(g),已知p(O2)=100kPa,p(NO)=1.01325kPa,p(NO2)=0.10325kPa。试通过计算说明,373K时反应能否自发进行?
第2题
A.NO2全部转化为N2O4
B.该反应已达化学平衡状态
C.正、逆反应速率相等,但不等于零
D.容器中气体颜色不再发生变化
第4题
A.正反应生成NO2的速率和逆反应生成O2的速率相等
B.反应容器中压强不随时间变化而变化
C.混合气体颜色深浅保持不变
D.混合气体平均相对分子质量保持不变
第5题
A.①②③
B.④⑤⑥
C.全部
D.①④⑥
第6题
A、CO + NO2 CO2 + NO ;
CO2 + NO ;
B、2NO2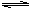
 2CO2 + 2NO (慢) ;
2CO2 + 2NO (慢) ;
C、2NO2 2NO + O2 (慢),2CO + O2
2NO + O2 (慢),2CO + O2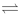 2CO2 (快) 。
2CO2 (快) 。
D、2NO2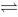 2NO + O2 (快),2CO + O2
2NO + O2 (快),2CO + O2 2CO2 (慢) 。
2CO2 (慢) 。
第7题
密闭容器中反应 2NO(g)+O2(g) 2NO2(g)在1500K条件下达到平衡。若始态p(NO)=150kPa,p(O2)=450kPa,p(NO2)=0;平衡时p(NO2)=25kPa。试计算平衡时p(NO),p(O2)的分压及平衡常数KΘ。
2NO2(g)在1500K条件下达到平衡。若始态p(NO)=150kPa,p(O2)=450kPa,p(NO2)=0;平衡时p(NO2)=25kPa。试计算平衡时p(NO),p(O2)的分压及平衡常数KΘ。
第8题
NO2冷却到室温时,它本身就会按下式反应而生成一种二聚体N2O4:
2NO2→N2O4
现将高温下的NO2充人10.0L烧瓶,将此烧瓶冷却到25℃测得烧瓶中气体的总压力为50.65kPa,试求算NO2和N2O4的分压和物质的量分数各为多少.
第9题
已知四氧化二氮的分解反应为N2O4(g)===2NO2(g)。在298.15K时,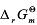 =4.75kJ·mol-1。试判断在此温度及下列条件下,反应进行的方向。
=4.75kJ·mol-1。试判断在此温度及下列条件下,反应进行的方向。
(1)N2O4(g,100kPa),NO2(g,100kPa);
(2)N2O4(g,1000kPa),NO2(g,100kPa);
(3)N2O4(g,300kPa),NO2(g,200kPa)。
第10题
已知 2NO(g)+O2(g)====2NO2(g)

计算298K时,上述反应的


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧