题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
某一立方晶系AB型金属氧化物,密度为3.581×103kg.m-3。今用波长为0.154nm的X射线测得在2θ为36.976°
、42.944°、62.36°、74.746°、78.686°、94.09。、105.806。、109.86。处有衍射峰,①该氧化物为何种点阵型式?②晶胞参数是多少?晶胞中的结构基元有几个?③金属原子占据何种空隙(正、负离子半径比为0.429)?④氧原子以何种方式堆积?⑤金属原子的相对原子质量是多少?⑥金属离子占据该种空隙的分数是多少?
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案


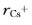 =169pm,rCl=181pm。如果认为Cs+和Cl-离子半径大致相近,那么这两种离子联合组成了何种型式的密堆积?画出示意图;④Cu2+处在何种空隙里?⑤Cu2+和Cs+对Cl-的配位数各是多少?
=169pm,rCl=181pm。如果认为Cs+和Cl-离子半径大致相近,那么这两种离子联合组成了何种型式的密堆积?画出示意图;④Cu2+处在何种空隙里?⑤Cu2+和Cs+对Cl-的配位数各是多少?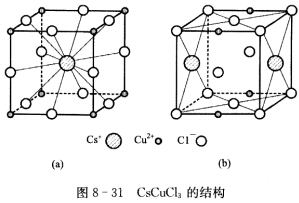
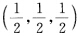 处,B原子在位置
处,B原子在位置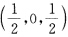 。①作图画出A、B原子的位置;②求AχBy晶胞中χ和y的数值;③若晶胞的边长为600pm,A和B相对原子质量分别为40和120,计算AχBy的密度;④考虑B原子,计算(100)、(110)、(111)面间距;⑤说明A和B的配位情况。
。①作图画出A、B原子的位置;②求AχBy晶胞中χ和y的数值;③若晶胞的边长为600pm,A和B相对原子质量分别为40和120,计算AχBy的密度;④考虑B原子,计算(100)、(110)、(111)面间距;⑤说明A和B的配位情况。