 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
写出下列原电池的电池反应,并计算25℃时的电动势和平衡常数KΘ。
写出下列原电池的电池反应,并计算25℃时的电动势和平衡常数KΘ。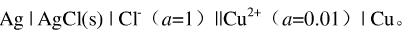
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
写出下列原电池的电池反应,并计算25℃时的电动势和平衡常数KΘ。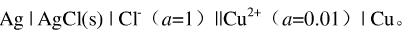
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“写出下列原电池的电池反应,并计算25℃时的电动势和平衡常数K…”相关的问题
更多“写出下列原电池的电池反应,并计算25℃时的电动势和平衡常数K…”相关的问题
第1题
在25℃时测得下列电池的电动势为0.28V
(-)Pt|H2(100kPa)|HAc(1mol·L-1),NaAc(1mol·L-1)||H+(1mol·L-1)|H2(100kPa)|Pt(+)
试计算25℃时HAc的。
第2题
将0.5000g含锌试样置于坩埚中灰化,其残渣溶于稀硫酸中,稀释后使锌转变成ZnC2O4沉淀,过滤洗涤后再用稀硫酸溶解沉淀,以0.02500mol·L-1的标准KMnO4溶液滴定,用去了35.00mL,计算ZnO的百分含量。[M(ZnO)=81.38g·mol-1]
第3题
已知EΘ(Pb2+/Pb)=-0.126V,EΘ(Fe3+/Fe2+)=0.771V,![]() (PbCl2)=1.6×10-5。在金属铅和硝酸铅溶液组成的半电池系统中,加入NaCl(aq),沉淀完全后。当c(Cl-)=1.0mol·L-1时,该半电池的电极电势是多少?将该半电池与Fe3+/Fe2+标准半电池组成原电池。写出原电池符号及电池反应的离子方程式,并计算此原电池的标准电动势EΘ。
(PbCl2)=1.6×10-5。在金属铅和硝酸铅溶液组成的半电池系统中,加入NaCl(aq),沉淀完全后。当c(Cl-)=1.0mol·L-1时,该半电池的电极电势是多少?将该半电池与Fe3+/Fe2+标准半电池组成原电池。写出原电池符号及电池反应的离子方程式,并计算此原电池的标准电动势EΘ。


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧