 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
计算298K时,如下反应的标准摩尔Gibbs自由能变化值和标准平衡常数。 H2(g)+I2(g)====2HI(g) 已知298K时,HI、
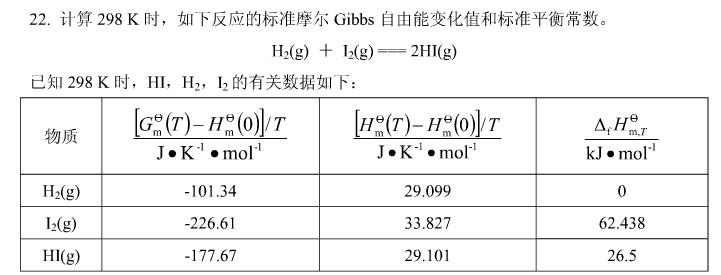
计算298K时,如下反应的标准摩尔Gibbs自由能变化值和标准平衡常数。
H2(g)+I2(g)====2HI(g)
已知298K时,HI、H2、I2的有关数据如下:
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
计算298K时,如下反应的标准摩尔Gibbs自由能变化值和标准平衡常数。
H2(g)+I2(g)====2HI(g)
已知298K时,HI、H2、I2的有关数据如下:

 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“计算298K时,如下反应的标准摩尔Gibbs自由能变化值和标…”相关的问题
更多“计算298K时,如下反应的标准摩尔Gibbs自由能变化值和标…”相关的问题
第3题
已知反应在298K的热力学数据如下:CO2(g)+H2=====CO(g)+H2O(g)
2010040 已知反应在298K的热力学数据如下:
CO2(g)+H2=====CO(g)+H2O(g)
ΔfH (kJ·mol-1) -393.5 0 -110.5 -241.8
求:
(1)298K时的反应的焓变;
(2)若此系统在400K时各组分气体的分压为p(CO)=p(H2O)=125kPa,p(CO2)=p(H2)=25kPa,通过计算判断反应进行的方向.已知298K时的平衡常数K=1.25
第4题
用配分函数计算298K时,如下反应的标准平衡常数。
H2(g)+I2(g)====2HI(g)
已知反应的,在298K时的参数如下表所示,忽略电子和核的贡献。
| 物质 | M/(kg·mol-1) | Θr/K | Θv/K |
| H2(g) | 2.0×10-3 | 85.4 | 6100 |
| I2(g) | 253.8×10-3 | 0.054 | 310 |
| HI(g) | 127.9×10-3 | 9.0 | 3200 |
第5题
计算5000K时,反应N2(g)====2N(g)的标准平衡常数。已知N2(g)分子的转动特征温度Θr=2.84K,振动特征温度Θv=3350K,解离能D=708.35kJ·mol-1,N2(g)的电子基态是非简并的,而N原子基态的简并度为4。
第6题
在N个NO分子组成的晶体中,每个分子都有两种可能的排列方式,即NO和ON,在0K时该体系的熵值为( )
A.S0=0 B.S0=kln2 C.S0=Nkln2 D.S0=2klnN
第7题
分子的平动、转动和振动的能级间隔的大小顺序是( )
A.振动能>转动能>平动能 B.振动能>平动能>转动能
C.平动能>振动能>转动能 D.转动能>平动能>振动能
第8题
在下列热力学函数的单粒子配分函数q统计表达式中,与系统的定位或非定位无关的是( )
A.G、F、S B.U、H、S C.U、H、Cv D.H、G、Cv
第9题
能量零点的不同选择对热力学量不产生影响的是( )
A.U、H、G B.U、H、S、Cv C.S、Cv D.S、F、G
第10题
在298K和100kPa时,摩尔平动熵最大的气体是( )
A.H2 B.CH4 C.NO D.CO2


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧