题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知在100kPa下,水的凝固点为0℃,在-5℃,过冷水的比凝固焓,过冷水和冰的饱和蒸气压分别为:ps(H2O,l)=0.422kPa
已知在100kPa下,水的凝固点为0℃,在-5℃,过冷水的比凝固焓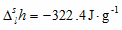 ,过冷水和冰的饱和蒸气压分别为:ps(H2O,l)=0.422kPa,ps(H2O,s)=0.414kPa。今在100kPa下,有-5℃过冷水1kg,变成同样温度、压力下的冰,设计可逆途径,并按可逆途径分别求出过程的△S及△G。
,过冷水和冰的饱和蒸气压分别为:ps(H2O,l)=0.422kPa,ps(H2O,s)=0.414kPa。今在100kPa下,有-5℃过冷水1kg,变成同样温度、压力下的冰,设计可逆途径,并按可逆途径分别求出过程的△S及△G。
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案