 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
原电池中关于盐桥的叙述错误的是 (A) 盐桥的电解质可中和两半电池中过剩的电荷 (B) 盐桥可维持氧化还原
原电池中关于盐桥的叙述错误的是
(A) 盐桥的电解质可中和两半电池中过剩的电荷
(B) 盐桥可维持氧化还原反应进行
(C) 电子通过盐桥流动
(D) 盐桥中的电解质不参与电极反应
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
原电池中关于盐桥的叙述错误的是
(A) 盐桥的电解质可中和两半电池中过剩的电荷
(B) 盐桥可维持氧化还原反应进行
(C) 电子通过盐桥流动
(D) 盐桥中的电解质不参与电极反应
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“原电池中关于盐桥的叙述错误的是 (A) 盐桥的电解质可中和两…”相关的问题
更多“原电池中关于盐桥的叙述错误的是 (A) 盐桥的电解质可中和两…”相关的问题
第1题
已知298K时下列电极电势: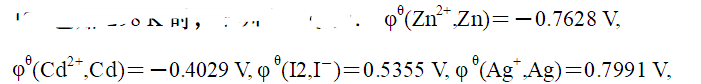 ,下列电池的标准电动势最大的是:
,下列电池的标准电动势最大的是:
(A) Zn(s)|zn2+||cd2+|Cd(s) (B) Zn(s)|zn2+||H+|H2,Pt
(C) Zn(s)|Z2+||I-|I2,Pt (D) Zn(s)|Zn2+||Ag+|Ag(s)
第2题
对原电池(-)Fe|Fe2+||Cu2+|Cu(+)随反应的进行,电动势将
(A) 变大 (B) 变小 (C) 不变 (D) 减小直至等于零
第7题
电极电势不随酸度变化的有
(A) O2/OH- (B) O2/H2O (C) Cl2/Cl- (D)
第8题
已知298K时,电极反应式
当c(H+)由1.0mol·dm-3减小到10-5时,该电对的电极电势变化值为
(A) 增加0.69V (B) 减少0.69V (C) 增加0.49V (D) 减少0.49V
第9题
下列几种水溶液,铜的电极电势E(Cu2+/Cu)最高的是
(A) 1.0mol·dm-3CuSO4溶液+浓氨水 (B) 1.0mol·dm-3CuSO4溶液+Na2S
(C) 金属铜在水中 (D) 1.0mol·dm-3CuSO4溶液
第10题
若算得电池反应的电池电动势为负值时,表示此电池反应是:
(A) 正向进行 (B) 逆向进行 (C) 不可能进行 (D) 反应方向不确定


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧