 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
空气中氧气氧化的半反应为:O2+4H++4e→2H2O,=1.23,理论上pH越高,氧气的电极电位越低。请说明:
空气中氧气氧化的半反应为:O2+4H++4e→2H2O,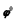 =1.23,理论上pH越高,氧气的电极电位越低。请说明:
=1.23,理论上pH越高,氧气的电极电位越低。请说明:

 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
空气中氧气氧化的半反应为:O2+4H++4e→2H2O,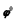 =1.23,理论上pH越高,氧气的电极电位越低。请说明:
=1.23,理论上pH越高,氧气的电极电位越低。请说明:

 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“空气中氧气氧化的半反应为:O2+4H++4e→2H2O,=1…”相关的问题
更多“空气中氧气氧化的半反应为:O2+4H++4e→2H2O,=1…”相关的问题
第1题
Co2+和Co3+与乙二胺配合物的结构性质如下:
| [Co(en)3]2+ | [Co(en)3]3+ | |
| 分裂能△o/cm-1 电子成对能P/cm-1 | 11000 19l00 | 23300 17800 |
请用晶体场理论推测[Co(en)3]2+和[Co(en)3]3+的磁性以及[Co(en)3]3+/[Co(en)3]2+电对的氧化还原能力。
第3题
在生命过程中,Fe(Ⅱ/Ⅲ)离子催化·OH生成反应:
催化还原:FeⅡL+H2O2→FeⅢL+·OH+OH-
催化氧化:FeⅢL+生物还原剂→FeⅡL+氧化产物
总反应:生物还原剂+H2O2→·OH+OH-+氧化产物
其中,氧化半反应:H2O2+H++e→·OH+H2O (H2O2/·OH)=0.32V
还原半反应:生物还原剂-ne→氧化产物 =-0.35~0.05V
因此,Fe(Ⅱ/Ⅲ)配离子催化上述反应的条件是其氧化还原电位处于-0.35~0.32V之间,这样既可以被H2O2氧化,又可以被生物还原剂还原。请计算下列哪种配体可以阻止上述反应发生:(1)EDTA;(2)吡咯二羧酸;(3)柠檬酸;(4)水杨酸;(5)邻菲罗啉。
已知:Fe3++e→Fe2+ =0.77V;
配合物稳定常数:
| EDTA(Y4-) | 吡咯二羧酸(Dipic2-) | 柠檬酸(Cit3-) | 水杨酸(Sal-) | 邻菲罗啉(o-Phen) | |
| Fe2+ | lgβ1=14.33 | 1gβ2=10.36 | lgβ1=15.5 | lgβ2=11.25 | lgβ3=21.3 |
| Fe3+ | lgβ1=24.23 | lgβ2=17.13 | lgβ1=25.0 | lgβ3=36.8 | lgβ3=23.5 |
第4题
用EDTA和EGTA为配体,可以制备什么范围的Ca2+缓冲溶液?今欲制备Ca2+总浓度为100μmoI·L-1,游离[Ca2+]=1.0μmol·L-1,pH=7.0的溶液100mL,问如何用储备液([Ca2+]=[EDTA]=[EGTA]=1.0mmol·L-1;pH=7.0的10×缓冲溶液)配制?已知:pH=7.0下,lgK's(Ca-EDTA)=7.60,lgK's(Ca-EGTA)=6.47。
第5题
μL,加入邻苯二甲醛显色剂4.0mL和1.5mL浓硫酸反应后,用1.00cm样品池测定550nm波长处吸光度分别为0.4803和0.6578。计算该血液样品中胆固醇的浓度。此人胆固醇浓度是否超标(正常范围:100~220mg/100mL)?
第6题
命名下列配离子和配合物,并指出中心原子及其配位数、配体和配位原子。
(1)[CoCl(NCS)(NH3)4]NO3
(2)[CoCl(NH3)5]Cl2
(3)[Al(OH)3]-
(4)[Co(en)3]Cl3
(5)[PtCl(NO2)(NH3)4]SO4
(6)K2Na[Co(ONO)6]
(7)Ni(CO)4
(8)Na3[Ag(S2O3)2]
第8题
以下各配合物中心原子的配位数均为6,假定它们的浓度都是0.0010mol·L-1,试指出各溶液导电能力大小的顺序,并解释之:
(1)[CrCl2(NH3)4]Cl
(2)[Pt(NH3)6]Cl4
(3)K2[PtCl6]
(4)[Co(NH3)6]Cl3
第9题
将Cr(Ⅲ),NH3,Cl-和K+组合在一起可以形成一系列7种配合物,其中的一种配合物是[Cr(NH3)6]Cl3。
(1)写出此系列中的其他6种配合物;
(2)命名每一种配合物。


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧