 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
项目管理信息系统中进度控制子系统的功能包括()。
A.进度计划执行情况的比较分析
B.编制资源需求计划
C.绘制网络图和计划横道图
D.确定合理工期
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.进度计划执行情况的比较分析
B.编制资源需求计划
C.绘制网络图和计划横道图
D.确定合理工期
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“项目管理信息系统中进度控制子系统的功能包括()。A.进度计划…”相关的问题
更多“项目管理信息系统中进度控制子系统的功能包括()。A.进度计划…”相关的问题
第1题
已知四氧化二氮的分解反应为N2O4(g)===2NO2(g)。在298.15K时,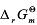 =4.75kJ·mol-1。试判断在此温度及下列条件下,反应进行的方向。
=4.75kJ·mol-1。试判断在此温度及下列条件下,反应进行的方向。
(1)N2O4(g,100kPa),NO2(g,100kPa);
(2)N2O4(g,1000kPa),NO2(g,100kPa);
(3)N2O4(g,300kPa),NO2(g,200kPa)。
第2题
Calculateat 298.15K for the reaction 2NO2(g)→N2O4(g). Is this reaction spontaneous?
第3题
若 298K 时反应N2O4 (g) = 2NO2(g) 的 Kө =0.1132,则当 N2O4 和 NO2 的分压均为1.0 kPa 时, 该反应()
A向生成 NO2 的方向进行
B向生成 N2O4 的方向进行
C正好达到化学平衡
D难于判断其进行方向
第4题
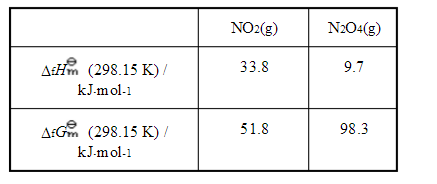
已知反应2NO2(g)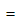 N2O4(g)及下表热力学数据,试计算该反应在298.15K和1000K时标准平衡常数
N2O4(g)及下表热力学数据,试计算该反应在298.15K和1000K时标准平衡常数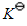 。
。
第5题
298 K时,反应N2O4(g)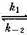 2NO2(g)的速率常数
2NO2(g)的速率常数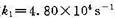 ,已知N2O4(g)和NO2(g)的标准摩尔生成Gibbs自由能分别为
,已知N2O4(g)和NO2(g)的标准摩尔生成Gibbs自由能分别为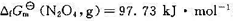 和
和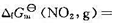 51.25 kJ·mol-1。请计算:(1)在298 K时,N2O4(g)的初始压力为100 kPa,NO2(g)的平衡分压;(2)该反应的弛豫时间r。
51.25 kJ·mol-1。请计算:(1)在298 K时,N2O4(g)的初始压力为100 kPa,NO2(g)的平衡分压;(2)该反应的弛豫时间r。
第6题
N2O5(g)→N2O4(g)+(1/2)O2(g)为一级反应。在25℃时,反应速率常数为0.0010min-1。同温度下产物N2O4能分解成NO2(g),并很快达平衡:N2O4(g) 2NO2(g),反应平衡常数
2NO2(g),反应平衡常数。今在25℃将压力为26.65kPa的N2O5置于一真空容器中,试求200min时容器中N2O5、O2、N2O4和NO2的分压力。
第7题
在1.013×105Pa下测得N2O4(g)在60℃时有50%离解,计算反应N2O4(g) 2NO2(g)的Kp。
2NO2(g)的Kp。
第8题
A.向生成NO2的方向进行
B.正好达到平衡
C.向生成N2O4的方向进行
D.难以判断其进行方向


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧