 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
在建筑面积与基地面积比值是一定的条件下,正确的是( )
A.建高层会增大建筑密度
B.建高层可以扩大绿化用地
C.建低层会减小建筑密度
D.建低层可以扩大绿化用地
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.建高层会增大建筑密度
B.建高层可以扩大绿化用地
C.建低层会减小建筑密度
D.建低层可以扩大绿化用地
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“在建筑面积与基地面积比值是一定的条件下,正确的是() A.建…”相关的问题
更多“在建筑面积与基地面积比值是一定的条件下,正确的是() A.建…”相关的问题
第1题
 ,在781 K时反应物的起始浓度:[H2] = 0.040
,在781 K时反应物的起始浓度:[H2] = 0.040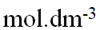 ,[I2]=0.050
,[I2]=0.050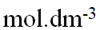 ,当[H2]减少一半时,反应速率是起始反应速率的:
,当[H2]减少一半时,反应速率是起始反应速率的:A.0.40倍
B.0.50倍
C.0.60倍
D.0.30倍
第2题
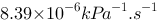 ;在1000 K时,速率常数为
;在1000 K时,速率常数为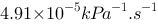 。则反应的活化能为:()
。则反应的活化能为:()A、100.5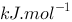
B、150.8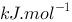
C、132.2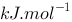
D、168.7 kJ . mol^{-1}
第3题
第4题
已知298K时的数据如下表:
物质 | H2(g) | I2(g) | HI(g) |
Delta_{f}G_{m}^{Theta }/(kJcdot mol^{-1}) | 0 | 19.359 | 1.7 |
求反应H2(g)+I2(g) 2HI(g)在298K时的
2HI(g)在298K时的。
第5题
用配分函数计算298K时,如下反应的标准平衡常数。
H2(g)+I2(g)====2HI(g)
已知反应的,在298K时的参数如下表所示,忽略电子和核的贡献。
| 物质 | M/(kg·mol-1) | Θr/K | Θv/K |
| H2(g) | 2.0×10-3 | 85.4 | 6100 |
| I2(g) | 253.8×10-3 | 0.054 | 310 |
| HI(g) | 127.9×10-3 | 9.0 | 3200 |
第6题
HI(g)的分解反应在836K时其速率常数k=0.00105s-1,在943K时的速率常数k=0.00268s-1。试计算:
(1)该反应的活化能Ea;
(2)在773K时的速率常数k。
第7题
已知反应:C2H5Br(g)→C2H4(g)+HBr(g),其活化能是226 kJ.mol-1,650 K时,速率常数为2.0×10-5s-1,试计算在哪个温度时速率常数是6.0×10-5s-1?
第8题
碘化氢的分解反应为均相二级反应 2HI(g)=H2(g)+I2(g) 已知反应的活化能Ea为185kJ.mol-1,分子的碰撞直径为3.50×10-10m。试确定反应速率常数kHI与温度的关系式并求556K时的反应速率常数。


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧