 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
实用主义教育学的主要观点是()。
A.以儿童为中心
B.重视学生在教学过程中的独立发现
C.学校即社会
D.以经验为中心组织课程
E.教育即学生经验的持续不断的增长
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.以儿童为中心
B.重视学生在教学过程中的独立发现
C.学校即社会
D.以经验为中心组织课程
E.教育即学生经验的持续不断的增长
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“实用主义教育学的主要观点是()。”相关的问题
更多“实用主义教育学的主要观点是()。”相关的问题
第1题
50ml、0.1mol/L的某一元己弱酸HA溶液与20ml、0.10mol/L的KOH溶液混合,并加水稀释至100ml,测得该溶液的pH=5.25。此一元弱酸的电离常数为()。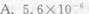
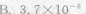
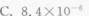
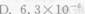
第2题
A.100mL 0.10mol/L KH2PO4溶液和50mL 0.10mol/L NaOH溶液
B.100mL 0.10mol/L HAc溶液和50mL 0.10mol/L NaOH溶液
C.100mL 0.10mol/L NaH2PO4溶液和50mL 0.20mol/L NaOH溶液
D.100mL 0.10mol/L KH2PO4溶液和50mL 0.10mol/L HCl溶液
E.含有0.1mol/LNaOH和0.1mol/LKCl的溶液
F.0.1mol/LNH3·H2O溶液与0.1mol/LHCl溶液的等体积混合液
第3题
取0.10mol·L-1的某一元弱酸(HA)50.0mL与20.0mL、0.10mol·L-1KOH溶液混合,将混合溶液稀释至100mL,测得此溶液的pH值为5.25,问此一元弱酸的Ka值是多少?
第4题
取50.00mL 0.10mol·L-1某一元弱酸溶液,与20mL 0.10mol·L-1NaOH溶液混合后,稀释到100mL。测此溶液的pH=5.25,计算此一元弱酸的Ka。
第5题
某一元弱酸HA,,现有0.10mol·L-1HA溶液1000mL,求该溶液的pH。若在此1000mLHA溶液中,加入0.1mol·L-1NaOH溶液400mL,求混合液的pH。
第8题
c(H+)=0.1mol/L的溶液50mL与c(OH-)=0.3mol/L的溶液50mL混合后,pH值为()。


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧