 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
实验测得反应:2A+B→2C+D的速率方程为:r=k[A],反应历程为:A+B→C+F(慢,k1),A+F→C+D(快,k2),则k1与k的关系为()
A.k=k1
B.2k=k1
C.k=2k1
D.k=k1-k2
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.k=k1
B.2k=k1
C.k=2k1
D.k=k1-k2
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“实验测得反应:2A+B→2C+D的速率方程为:r=k[A],…”相关的问题
更多“实验测得反应:2A+B→2C+D的速率方程为:r=k[A],…”相关的问题
第1题
A.k=k1
B.2k=k1
C.k=2k1
D.k=k1-k2
第2题
A.k=k1
B.2k=k1
C.k=2k1
D.k=k1-k2
第4题
一氧化碳与氯气在高温下作用得到光气(COCl2),实验测得反应的速率方程为
 有人解释其反应机理为
有人解释其反应机理为

(1)试说明这一机理与速率方程相符合;
(2)指出反应速率方程中的k与反应机制中的速率常数(k1、k-1、k2、k-2)间的关系。
第5题
在473K时,有反应A+2B→2C+D,其速率方程可写成r=k[A]x[B]y。实验(1):当A、B的初始浓度分别为[A]0=0.01mol·dm-3和[B]0=0.02mol·dm-3时,测得反应物B在不同时刻的浓度数据如下:
| t/h | 0 | 90 | 217 |
| [B]/(mol·dm-3) | 0.020 | 0.010 | 0.0050 |

第6题
Lindemann 单分子反应理论认为,单分子反应的历程为
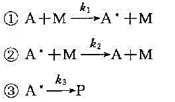
(1)请用推导证明,反应速率方程为r=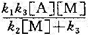 。
。
(2)请应用简单碰撞理论计算469℃时的k1,已知2-丁烯的d=0.5 nm,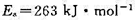 ;
;
(3)若反应速率方程写成r=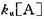 ,且
,且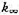 为高压极限时的表观速率常数,请计算
为高压极限时的表观速率常数,请计算 的压力P1/2,已知
的压力P1/2,已知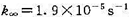 ;
;
(4)实验测得丁烯异构化在469℃时的p1/2=0.532 Pa,试比较理论计算的p1/2(理论)与实验值p1/2(实验)之间的差异,对此你有何评论?
第7题
反应A+B→C+D的速率方程为r=k[A][B],则反应
A、是二分子反应
B、是二级反应但不一定是二分子反应
C、不是二分子反应
D、是对A、B各为一级的二分子反应
第8题
一氧化碳与氯气在高温下作用得到光气: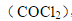 ,实验测得反应的速率方程为
,实验测得反应的速率方程为
d[COCl2]/dt=k[CO][Cl2]3/2
有人提出其反应机理为:



为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧