 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
醋酸的解离平衡常数Ka^Ө=1.76×10^-5。在此温度下浓度分别为0.050 mol/L和0.010 mol/L的醋酸溶液,分别求算这两种溶液中醋酸的解离度和pH值。
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“醋酸的解离平衡常数Ka^Ө=1.76×10^-5。在此温度下…”相关的问题
更多“醋酸的解离平衡常数Ka^Ө=1.76×10^-5。在此温度下…”相关的问题
第1题
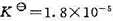 ,试计算在下列不同情况下醋酸在浓度为1.0mol·kg-1时的解离度。(1)设溶液是理想的,活度因子均为1;(2)用Debye-Huckel极限公式计算出γ±的值,然后再计算解离度。设未解离的HAc的活度因子为1.
,试计算在下列不同情况下醋酸在浓度为1.0mol·kg-1时的解离度。(1)设溶液是理想的,活度因子均为1;(2)用Debye-Huckel极限公式计算出γ±的值,然后再计算解离度。设未解离的HAc的活度因子为1.
第2题
 的平衡常数为2.8×10-9,醋酸自解离反应
的平衡常数为2.8×10-9,醋酸自解离反应 的离子积为3.6×10-15。试计算含有1.0×10-4mol·L-1HCl的醋酸溶液中HCl,H2Ac+,Cl-和Ac-的浓度。
的离子积为3.6×10-15。试计算含有1.0×10-4mol·L-1HCl的醋酸溶液中HCl,H2Ac+,Cl-和Ac-的浓度。
第3题
某温度下,反应![]() 的平衡常数
的平衡常数![]() =1.0,同温度下,若B2+和A2+的浓度分别为0.50mol·L-1和0.10mol·L-1,则( )
=1.0,同温度下,若B2+和A2+的浓度分别为0.50mol·L-1和0.10mol·L-1,则( )
A.正向反应是自发的 B.系统处于平衡状态
C.逆向反应是自发的 D.无法判断反应方向
第4题
某一元弱酸HA的浓度为0.010mol·L-1,在常温下测得其pH为4.0。求该一元弱酸的解离平衡常数和解离度。
第5题
在523K时,将0.110mol的PCI5(g)引入1L容器中建立
PCl5(g)=PCl3(g)+Cl2(g)
平衡时PCI3(g)的浓度为0.050mol·L-1,试求:
(1)平衡时PCI3和Cl2的分压为多少?
(2)在523K时的标准平衡常数Kp为多少?
第7题
 的平衡常数为2.8×10-9,醋酸自解离反应
的平衡常数为2.8×10-9,醋酸自解离反应 的离子积为3.6×10-15。试计算含有1.0×10-4mol·L-1HCl的醋酸溶液中HCl,H2Ac+,Cl-和Ac-的浓度。
的离子积为3.6×10-15。试计算含有1.0×10-4mol·L-1HCl的醋酸溶液中HCl,H2Ac+,Cl-和Ac-的浓度。


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧