 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
4.根据初中或高中的化学教材内容(各个版本都可以),选择其中一个课时,进行教学方案设计。要求: (1) 分析本课时教材的地位和作用。(6分) (2)确定本节课的三维教学目标并规范陈述。(9分) (3) 确定本课的教学重点和难点,并说明如何突出重点和突破难点的?(10分) (4) 设计本课时的教学过程,要求说明教师活动、学生活动和设计意图。(25分) (5) 试对本课教学内容进行板书设计。(5分)
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“4.根据初中或高中的化学教材内容(各个版本都可以),选择其中…”相关的问题
更多“4.根据初中或高中的化学教材内容(各个版本都可以),选择其中…”相关的问题
第2题
材料一《普通高中化学课程标准(实验)》关于“难溶电解质的溶解平衡”的内容标准是:能描述沉淀溶解平衡,知道沉淀转化的本质。
材料二某版本高中实验教科书《化学4》“难溶电解质的溶解平衡”的部分内容:
二、沉淀反应的应用
难溶电解质的溶解平衡也是动态平衡.同样可以通过改变条件使平衡移动——溶液中的离子转化为沉淀,或沉淀转化为溶液中的离子。
1.沉淀的生成
在涉及无机制备、提纯工艺的生产、科研、废水处理等领域中.常利用生成沉淀来达到分离或除去某些离子的目的。例如,工业原料氯化铵中含杂质氯化铁,使其溶解于水,再加入氨水调节pH至7~8,可使Fe3+生成Fe(OH)3沉淀而除去。除调节pH使生成氢氧化物沉淀外,以Na2s、H2s等作沉淀剂,使某些金属离子如Cu2+、Hg2+等,生成极难溶的硫化物CuS、HgS等沉淀,也是分离、除去杂质常用的方法。 .
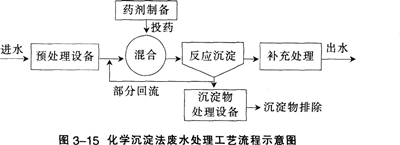
思考与交流
利用生成沉淀分离或除去某种离子,首先要使生成沉淀的反应能够发生:其次希望沉淀生成的反应进行得越完全越好。
1.如果要除去某溶液中的S042-你选择加入钙盐还是钡盐?为什么?
2.以你现有的知识,你认为判断沉淀能否生成可从哪些方面考虑?是否可能使要除去的离子全部通过沉淀除去?说明原因。
材料三教学对象为高中二年级学生,他们已经学习了必修化学1、必修化学2和“化学反应与能量”“化学反应速率和化学平衡”以及“弱电解质的电离”“水的电离和溶液的酸碱度”“盐类的水解”等知识。
要求:
(1)回答材料二中“思考与交流”中的问题。
(2)完成“难溶电解质的溶解平衡”的教学设计,内容包括教学重难点、教学方法和教学过程。
第3题
材料一《普通高中化学课程标准(实验)》关于“几种重要的金属化合物”的内容标准是:根据生产、生活中的应用实例或通过实验探究,了解钠、铝、铁、铜等金属及其重要化合物的主要性质.能列举合金材料的重要应用。
材料二某版本高中实验教科书《化学1》“钠的重要化合物”的部分内容:
氧化钠和过氧化钠思考与交流
1.回忆前面做过的实验.描述氧化钠和过氧化钠的颜色、状态。
2.氧化钠与水的反应和氧化钙与水的反应类似,请你写出氧化钠与水反应的化学方程式。
实验3—5
把水滴入盛有少量过氧化钠固体的试管中,立即把带火星的木条放在试管口,检验生成的气体。用手轻轻摸一摸试管外壁,有什么感觉?然后向反应后的溶液中滴入酚酞溶液.有什么现象发生?
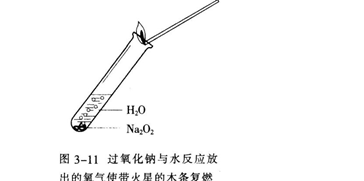
通过实验和观察.请你描述一下这些现象。过氧化钠与水反应生成氢氧化钠和氧气:2Na202+2H20=4NaOH+02↑
过氧化钠还能与二氧化碳反应生成碳酸钠和氧气:2Na202+2C02==2Na2C03+02↑
因此.过氧化钠可用于呼吸面具或潜水艇中氧气的来源。
材料三教学对象为高中一年级学生.他们已经学习了必须化学1的“从实验学化学…‘化学物质及其变化”和“金属的化学性质”等知识。
要求:
(1)回答材料二中“思考与交流”中的问题。
(2)完成“氧化钠和过氧化钠”的教学设计片段,内容包括教学目标、教学重难点和教学过程。并对教学过程做简要说明。(不少于300字)
第4题
A.钻研教材
B.了解学生
C.制订教学进度计划
D.写好教学反思
第5题
高中课程要成为每个学生个性发展和走向自立的平台,要体现基础性、时代性和选择性。虽然每一个化学课程模块的内容线索、侧重面及对学生的学习要求并不相同,但各模块内容之间存在着一定的内在联系。
问题:
(1)高中化学课程分为哪几个模块?
(2)各个模块之间存在怎样的关系?
第6题
阅渎下列三段高中化学教学中有关“铁的重要化合物”的材料。
材料一《普通高中课程标准(实验)》的内容标准:根据生产、生活中的应用实例或通过实验探究,了解钠、铝、铁、铜等金属及其重要化合物的主要性质,能列举合金材料的重要应用。
材料二“铁的重要化合物”内容属于高中化学必修阶段的无机元素化合物教学内容,必修化学课程中的无机元素化合物知识安排在《化学1》的“主题3常见无机物及其应用”中。普通高中课程标准使用教科书《化学1》的目录:
第一章从实验学化学
第二章化学物质及其变化
第三章金属及其化合物
第一节金属的化学性质
第二节几种重要的金属化合物
第三节用途广泛的金属材料
第四章非金属及其化合物
材料三以下是某教师设计的教学活动:
【学生活动】阅读教材关于铁的氧化物的介绍,利用分类法归纳FeO、Fe2O3、Fe3O4的性质,并填写表格。
【学生实验1】氢氧化铁、氢氧化亚铁的制备与Fe3+离子检验(整合实验)。
【问题情景1】阅读课文,结合实验现象,思考与讨论:
1.利用KSCN溶液,可以根据什么现象检验溶液中Fe3+的存在?Fe2+离子遇到KSCN会产生相同的现象吗?
2.FeSO4溶液滴加KSCN溶液一段时间后,再次观察溶液的颜色,出现了什么变化?该变化说明了什么?由此你可以得出什么结论?
3.Fe(OH)2沉淀是什么颜色?为什么往FeSO4溶液中滴加NaOH溶液后生成的沉淀会出现颜色变化?
【师生小结】
【问题情景2】
1.从Fe2+被O2氧化为Fe3+,体现了Fe2+的什么性质?除了O2,还有哪些物质可以氧化Fe2+?
2.若要实现从Fe3+转为Fe2+的变化,需要加入什么物质?
【学生实验2】Fe2+与Fe3+的转化,按照教材P)61科学探究进行实验,观察与记录实验现象。
【问题情景3】结合实验探究的现象,思考与讨论:
l.Fe3+与铁粉充分反应后的产物是什么?如何证明?
2.回忆前面有关Fe2+的实验,为什么用Fe与稀硫酸制备FeSO4溶液,并保持铁过量?
3.实验中如何判断Fe3+已充分反应?反应不充分对实验结果有何影响?
【师生小结】
【问题情景3】学生课后思考与讨论
通过学习我们知道,Fe2+离子和Fe(OH)2中+2价的铁均易被氧化。根据所学的知识,思考:利用FeSO4溶液和NaOH溶液时,如何通过实验条件的控制,制备较纯净的Fe(OH)2白色沉淀?
请根据上述材料,完成“铁的化合物”这一教学片段的有关任务:
问题:
(1)试确定本课的三维教学目标。
(2)说明本节课的教学策略。
(3)请对本课内容进行板书设计。
(4)请对本课内容设计导入。
(5)请写出氢氧化铁、氢氧化亚铁的制备与检验Fe3+离子的实验步骤。


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧