 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
用Nernst方程式计算Br₂/Br-电对的电极电势,下列叙述中正确的是
A.Br₂ 的浓度增大,j 增大
B.Br-的浓度增大,j 减小
C.H+浓度增大,j 减小
D.温度升高对j 无影响
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.Br₂ 的浓度增大,j 增大
B.Br-的浓度增大,j 减小
C.H+浓度增大,j 减小
D.温度升高对j 无影响
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“用Nernst方程式计算Br₂/Br-电对的电极电势,下列叙…”相关的问题
更多“用Nernst方程式计算Br₂/Br-电对的电极电势,下列叙…”相关的问题
第1题
A.温度应为298K
B.H+浓度的变化对φ的影响比Mn2+浓度变化的影响大
C.φ与得失电子数无关
D.Mn2+浓度增大时φ增大
第2题
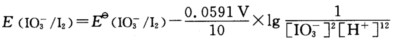 当把[H+]换成pH,而其他物质的浓度都为标准态浓度,则有
当把[H+]换成pH,而其他物质的浓度都为标准态浓度,则有
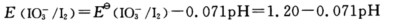 再由E对pH作图,即得E-pH图。根据如下E-pH图(坐标未按比例),回答问题:
再由E对pH作图,即得E-pH图。根据如下E-pH图(坐标未按比例),回答问题:
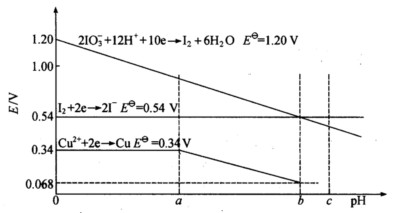 (1)写出由IO3-/I2及I2/I-发生的氧化还原反应的方程式; (2)当pH为a、6、C时,分别指出(1)中反应所进行的方向; (3)计算上述反应的
(1)写出由IO3-/I2及I2/I-发生的氧化还原反应的方程式; (2)当pH为a、6、C时,分别指出(1)中反应所进行的方向; (3)计算上述反应的
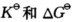 (298 K); (4)计算pH=b时的b值,此时反应的
(298 K); (4)计算pH=b时的b值,此时反应的
 为多少? (5)E(Cu2+/Cu)的E-pH图从a开始变成了斜率为负的斜线,原因何在? (6)根据图中的数据,求Cu(OH)2的Ksp。
为多少? (5)E(Cu2+/Cu)的E-pH图从a开始变成了斜率为负的斜线,原因何在? (6)根据图中的数据,求Cu(OH)2的Ksp。
第3题
B 、电对的电极电势越大,电对中的还原型物质是越强的还原剂
C 、电对的电极电势越小,电对中的还原型物质是越强的还原剂
D、电对的电极电势越大.电对中的氧化型物质是越的氧化剂
第4题
B、H+浓度的变化对E的影响比Mn2+浓度变化的影响大
C、E和得失电子数无关
D、MnO4-浓度增大时E增大
第5题
B.条件电势是任意浓度下的电极电势
C.条件电势是电对氧化态和还原态浓度均等于1mol·L-1
D.条件电势是在一定条件下,电对氧化态和还原态总浓度均为1mol·L-1,校正了各种外界因素影响的实际电势


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧