 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
参加化学反应的各物质的质量总和不等于反应后生成的各物质的质量总和。
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“参加化学反应的各物质的质量总和不等于反应后生成的各物质的质量…”相关的问题
更多“参加化学反应的各物质的质量总和不等于反应后生成的各物质的质量…”相关的问题
第4题
第5题
(1)在速率方程中,各物质浓度的幂次等于反应式中各物质化学式前的计量系数时,该反应即为元反应。
(2)单分子反应是一级反应,双分子反应是二级反应。
(3)反应的级数与反应的分子数是同义词。
(4)在反应途径中,控速步骤是反应速率最慢的一步。
(5)温度升高使反应速率加快是由于温度升高使分子碰撞频率增大,从而使反应速率加快。
(6)两个不同的反应相比,活化能大的,其反应速率一定慢。
(7)有了化学方程式,我们就能够根据质量作用定律写出它的速率方程。
(8)催化剂对正、逆反应的速率影响是一样的。
(9)任何反应的反应速率都是随时间变化的。
(10)反应速率常数的大小就是反应速率的大小。
(11)从反应速率常数的单位可以判断该反应的级数。
(12)逆反应的活化能在数值上等于正反应的活化能,只不过符号相反而已。
(13)对于同一个反应,加入的催化剂虽然不同,但活化能的降低是相同的。
第6题
A.反应前后物质的种类没有变化
B.反应前后原子的种类和数目没有变化
C.反应前后分子的种类和数目没有变化
D.反应前后元素的种类没有变化
第7题
试讲题目
1.题目:质量守恒定律
2.内容:
探究反应前后物质的质量关系
当物质发生化学反应生成新物质时,反应物的质量总和与生成物的质量总和相比较,存在什么关系?
根据以下实验方案分组进行实验,并将实验结果填入表中。
请你在实验中观察和探究以下问题,并结合条件思考和作出分析:
(1)反应物和生成物的状态及其他变化;
(2)实验中观察到的质量变化情况。
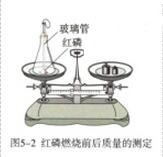
方案一:在底部铺有细沙的锥形瓶中,放入一小堆干燥的玻璃管红磷。在锥形瓶口的橡胶塞上安装一根玻璃管,在其上端系牢红磷一个小气球,并使玻璃管下端能与红磷接触。将锥形瓶和玻璃管放在托盘天平上用砝码平衡,记录所称的质量m1。然后,取下锥形瓶,将橡胶塞上的玻璃管放到酒精灯火焰上灼烧至红热后,迅速用橡胶塞将锥形瓶塞紧,并将红磷引燃。待锥形瓶冷却后,重新放到托盘天平上,记录所称的质量m2。
方案二:在锥形瓶中加入适量稀硫酸铜溶液,塞好橡胶塞。将几根铁钉用砂纸打磨干净,将盛有硫酸铜溶液的锥形瓶和铁钉一起放在托盘天平上称量,记录所称的质量m1。将铁钉浸在硫酸铜溶液中,观察实验现象。待反应一段时间后溶液颜色改变时,将盛有硫酸铜溶液和铁钉的锥形瓶放在托盘天平上称量,记录所称的质量m2。比较反应前后的质量。

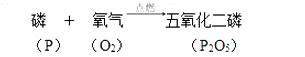
铁与硫酸铜的反应可表示如下:

讨论:分析两个方案的实验结果,你得到什么结论?
大量实验证明,参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。这个规律叫做质量守恒定律。
3基本要求:
(1)配合教学内容要有适当板书。
(2)教学中要有提问互动环节。
(3)教学中的实验用语言进行情景模拟。
答辩题目
1.请你说出本节课的教学目标?
2.根据质量守恒定律解释:镁在氧气中燃烧后生成物的质量比原来镁条的质量大。


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧