 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在1273K,总压力为30p0,反应CO2(g)+C(s)⇌2CO(g)达到平衡,在此温度下保持总压不变加入N2气,使N2
在1273K,总压力为30p0,反应CO2(g)+C(s)⇌2CO(g)达到平衡,在此温度下保持总压不变加入N2气,使N2气的分压达到20标准大气压,则加入N2气后的平衡将向左移动。()
此题为判断题(对,错)。
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在1273K,总压力为30p0,反应CO2(g)+C(s)⇌2CO(g)达到平衡,在此温度下保持总压不变加入N2气,使N2气的分压达到20标准大气压,则加入N2气后的平衡将向左移动。()
此题为判断题(对,错)。
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“在1273K,总压力为30p0,反应CO2(g)+C(s)⇌…”相关的问题
更多“在1273K,总压力为30p0,反应CO2(g)+C(s)⇌…”相关的问题
第1题
CO2(g)与H2S(g)在高温的反应为CO2(g)+H2S(g)===COS(g)+H2O(g),今在610K时将4.4g的CO2(g)加入体积为2.5dm3的空瓶中,然后再充入H2S(g)使总压为1000kPa。达平衡后取样分析,得其中H2O(g)的摩尔分数为0.02。将温度升至620K重复上述实验,达平衡后取样分析. 得其中H2O(g)的摩尔分数为0.03。视气体为理想气体,试计算:
(1)610K时的![]() ;
;
(2)610K时的![]() ;
;
(3)反应的标准摩尔焓变![]() (设其不随温度而变);
(设其不随温度而变);
(4)610K时,往该体积的瓶中充入不参与反应的气体,直至压力加倍,则COS(g)的产量有何变化。若充入不参与反应的气体,保持压力不变,而使体积加倍,COS(g)的产量又有何变化。
第2题
(1)2NaHCO3(s)===Na2CO3(s)+H2O(g)+CO2(g)
(2)CuSO4·5H2O(s)===CuSO4·3H2O(s)+2H2O(g)
已知反应(1)的解离压力为4.0kPa,反应(2)的水气压力为6.05kPa。试计算由NaHCO3(s)、Na2CO3(s)、CuSO4·5H2O(s)和CuSO4·3H2O(s)所组成的系统,在达到同时平衡时CO2(g)的分压。
第3题
 2NH3(g)+CO2(g)的KpΘ。
2NH3(g)+CO2(g)的KpΘ。
第4题
第5题
此题为判断题(对,错)。
第6题
在通常温度下,NH4HCO3(s)可发生下列分解反应:
NH4HCO3(s)==NH3(g)+CO2(g)+H2O(g)
设在两个容积相等的密闭容器Ⅰ和Ⅱ中,开始分别盛有纯NH4HCO3(s) 1kg及20kg,均保持在298K。达到平衡后,下列哪种说法是正确的? ( )
A.两容器中压力相等 B.容器Ⅰ内的压力大于容器Ⅱ内的压力
C.容器Ⅱ内的压力大于容器Ⅰ内的压力 D.须经实际测定方能判别哪个容器中压力大
第7题
 ,今在610 K时将4.4 g的CO2(g)加入体积为2.5 dm3的空瓶中,然后再充入H2S(g)使总压为1000 kPa.达平衡后取样分析,得其中H2O(g)的摩尔分数为0.02。将温度升至620K重复上述实验,达平衡后取样分析,得其中H2O(g)的摩尔分数为0.03。视气体为理想气体,试计算:
,今在610 K时将4.4 g的CO2(g)加入体积为2.5 dm3的空瓶中,然后再充入H2S(g)使总压为1000 kPa.达平衡后取样分析,得其中H2O(g)的摩尔分数为0.02。将温度升至620K重复上述实验,达平衡后取样分析,得其中H2O(g)的摩尔分数为0.03。视气体为理想气体,试计算:(1) 610K时的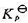 ;
;
(2)610K时的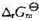 ;
;
(3)反应的标准摩尔焓变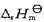 (设其不随温度而变);
(设其不随温度而变);
(4)610K时,往该体积的瓶中充人不参与反应的气体,直至压力加倍,则COS(g)的产量有何变化。若充入不参与反应的气体,保持压力不变,而使体积加倍,COS(g)的产量又有何变化。
第8题
1.jpg) (2)298K及标准压力下该生成反应达到平衡时C8H18(g)的摩尔分数; (3)讨论温度和压力对C8H18(g)生成反应的影响。
(2)298K及标准压力下该生成反应达到平衡时C8H18(g)的摩尔分数; (3)讨论温度和压力对C8H18(g)生成反应的影响。
第9题
①2NaHCO3(s)===Na2CO3(s)+H2O(g)+CO2(g)
②CuSO4·5H2O(s)===CuSO4·3H2O(s)+2H2O(g)
求:(1)反应①和②的和
;(2)将反应①,②中的四种固体物质放入一真空容器中,平衡后CO2的分压力为多少(T=323K)?


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧