 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
在27℃时,2mol的N2(假设为理想气体)从106Pa等温可逆膨胀到105Pa,试计算其△S.
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“在27℃时,2mol的N2(假设为理想气体)从106Pa等温…”相关的问题
更多“在27℃时,2mol的N2(假设为理想气体)从106Pa等温…”相关的问题
第2题
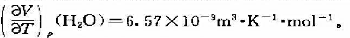
第3题
(2)若该气体由25℃、105Pa交到40℃、106Pa,求△H.
第4题
第5题


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧