 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
合成氨反应N2(g)+3H2(g)=2NH3(g),已知在25℃、Pθ下,ΔrGθm(298
合成氨反应N2(g)+3H2(g)=2NH3(g),已知在25℃、Pθ下,ΔrGθm(298K)
=-33.26kJ·mol-1,ΔrHθm(298K)=-92.38kJ·mol-1,假设此反应的ΔrHθm不随T而变化,试求算在500K时此反应的ΔrGθm,并说明温度升高对此反应是否有利.
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
合成氨反应N2(g)+3H2(g)=2NH3(g),已知在25℃、Pθ下,ΔrGθm(298K)
=-33.26kJ·mol-1,ΔrHθm(298K)=-92.38kJ·mol-1,假设此反应的ΔrHθm不随T而变化,试求算在500K时此反应的ΔrGθm,并说明温度升高对此反应是否有利.
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“合成氨反应N2(g)+3H2(g)=2NH3(g),已知在2…”相关的问题
更多“合成氨反应N2(g)+3H2(g)=2NH3(g),已知在2…”相关的问题
第1题
已知ΔfGm(NH3,g)=-16.45kJ·mol-1,计算合成氨反应
N2(g)+3H2(g)→2NH3(g)
在298.15K、标准状态时反应的标准平衡常数KΘ。
第5题
已知合成氨反应 N2(g)+3H2(g)=2NH3(g) 在298K、pθ下的△rGmθ=-33.26kJ.mol-1,△rGmθ=-92.38kJ.mol-1,假设此反应的△rGmθ不随T而变化,求500K时此反应的△rGmθ,并由计算结果说明温度对反应的影响。
第6题
已知

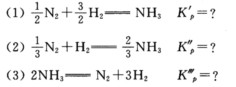
本题中4个Kp值的意义是否相同?讨论合成氨的反应时,是否可以用任意一种Kp?
第7题
已知N2+3H2=2NH3 Kp(673 K)=6.1×10-4。问此K户与下述3个K的意义是否相同?在进行合成氨反应的平衡计算时,是否可用任意一种Kp?
第9题
在实际生产中合成氨反应
N2+3H2 2NH3(a)
2NH3(a)
是在高温、高压下采用熔融铁催化剂进行的,合成氨反应为可逆放热反应,故过程尽可能按最佳温度曲线进行。已知该催化剂的正反应活化能为58.618×103J/mol,逆反应的活化能为167.48×103J/mol。平衡常数Kp与温度的T(单位为K)及总压p(单位为MPa)的关系为

现拟计算下列条件下的最佳温度:
第10题
合成氨反应:

在30.4MPa,500℃时,K为7.8×10-5,计算该温度时下列反应的K:


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧