题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
1500K时,CaCO3分解反应为CaCO3(s)=CaO(s)+CO2(g),平衡常数KΘ=0.50.10L真空
1500K时,CaCO3分解反应为CaCO3(s)=CaO(s)+CO2(g),平衡常数KΘ=0.50.10L真空容器中置有1molCaCO3(s),平衡时CaCO3部分分解,且生成的CO2分解CO2(g)=CO(g)+1/2O2(g),平衡时容器中O2的分压为15kPa.求1500K时CO2分解反应的平衡常数和CaCO3的分解率.设CO2、CO和O2都是理想气体.
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案



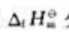 分别为-1207kJ·mol-1-635kJ·mol-1和-392kJ·mol-1,则298.15K时化学反应
分别为-1207kJ·mol-1-635kJ·mol-1和-392kJ·mol-1,则298.15K时化学反应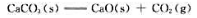 的标准摩尔焓变
的标准摩尔焓变 为().
为(). 。若将1.00 mol CaCO3装入1.00 dm3真空容器中,加热到1500 K达平衡时,气体混合物中O2的摩尔分数为0.15。计算容器中CaO的物质的量n(CaO)。
。若将1.00 mol CaCO3装入1.00 dm3真空容器中,加热到1500 K达平衡时,气体混合物中O2的摩尔分数为0.15。计算容器中CaO的物质的量n(CaO)。