 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
25℃时,电池反应的标准电动势为2.00V.实验测得该原电池的电动势为2.73V,则电池反应的为().A、
A.#图片2$#
B.#图片3$#
C.#图片4$#
D.#图片5$#
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.#图片2$#
B.#图片3$#
C.#图片4$#
D.#图片5$#
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“25℃时,电池反应的标准电动势为2.00V.实验测得该原电池…”相关的问题
更多“25℃时,电池反应的标准电动势为2.00V.实验测得该原电池…”相关的问题
第2题
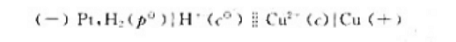
当c(Cu2+)=0.010mol·L-1时,实验测得原电池的电动势为0.28V。已知300K时,2.303RT/F=0.060V,计算300K时电对Cu2+/Cu的标准电极
第3题
PbSO4的Ksp可用如下方法测得:选择Cu2+/Cu,Pb2+/Pb两电对组成一个原电池,在Cu2+/Cu半电池中使c(Cu2+)=1.0mol·L-1,在Pb2+/Pb半电池中加入![]() ,产生PbSO4沉淀,并调至
,产生PbSO4沉淀,并调至![]() 。实验测得电动势E=0.62V(已知铜为正极),计算PbSO4的Ksp。
。实验测得电动势E=0.62V(已知铜为正极),计算PbSO4的Ksp。
第4题
(-)Pt|H2(100kPa)|HAc(1mol·L-1),NaAc(1mol·L-1)||H+(1mol·L-1)|H2(100kPa)|Pt(+)
试计算25℃时HAc的。
第6题
25℃时,下列电池的电动势为0.411V:
(—)镁离子电极|Mg2+(1.8×10-3mol·L-1)||饱和甘汞电极(+)
用含Mg2+试液代替已知浓度的溶液时,测得电池的电动势为0.439V,求试液中的pMg。
第7题
下述电池的溶液为pH=4.00的标准缓冲溶液,25℃时测得电动势为0.209V:
pH玻璃电极|H+(a=x)‖饱和甘汞电极
当分别用三种未知溶液代替标准缓冲溶液时,测得电动势为:①0.312V;②0.088V;③-0.017V。试计算每种溶液的pH及氢离子活度。
第8题
测得下列电池的电动势为0.972V(25℃):
(—)Cd|CdX2(s)|X-(0.0200mol·L-1)||SCE(+)
已知:![]() , φSCE=0.244V。计算CdX2的
, φSCE=0.244V。计算CdX2的![]() 。
。
第9题
A.1/10
B.1/100
C.10/1
D.100/1
第10题
当下列电池中的溶液是H=4.00时的缓冲溶液时,在25℃测得电池的电动势为0.209V。
(—)玻璃电极|H+(a=x)![]() 当缓冲溶液由未知溶液代替时,测得电池电动势如下: (1)0.312V; (2)0.098V;(3)=0.017V。试计算每种溶液的pH值。
当缓冲溶液由未知溶液代替时,测得电池电动势如下: (1)0.312V; (2)0.098V;(3)=0.017V。试计算每种溶液的pH值。


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧