 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
实验测得碳燃烧为二氧化碳和一氧化碳燃烧为二氧化碳的燃烧热 Q=-△H,其数值分别如下: 试根据
实验测得碳燃烧为二氧化碳和一氧化碳燃烧为二氧化碳的燃烧热

Q=-△H,其数值分别如下:
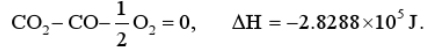
试根据赫斯定律计算碳燃烧为一氧化碳的燃烧热.
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
实验测得碳燃烧为二氧化碳和一氧化碳燃烧为二氧化碳的燃烧热

Q=-△H,其数值分别如下:
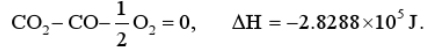
试根据赫斯定律计算碳燃烧为一氧化碳的燃烧热.
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“实验测得碳燃烧为二氧化碳和一氧化碳燃烧为二氧化碳的燃烧热 Q…”相关的问题
更多“实验测得碳燃烧为二氧化碳和一氧化碳燃烧为二氧化碳的燃烧热 Q…”相关的问题
第1题
二元理想溶液具有下列形式的化学势:
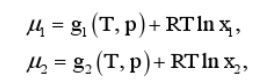
其中gi(T,p)为纯i组元的化学势,xi是溶液中i组元的摩尔分数.当物质的量分别为n1,n2的两种纯液体在等温等压下合成理想溶液时,试证明混合前后
(a)吉布斯函数的变化为
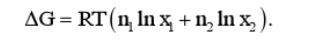
(b)体积不变,即△V=0.
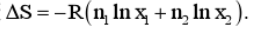
(c)熵变 (d)焓变AH=0,因而没有混合热.
(e)内能变化为多少?
第2题
第3题
核处在基态,而B气体的原子核处在激发态、已知核激发态的寿命远大于抽去隔板后气体在容器内的扩散时间,令容器与热源接触,保持恒定的温度.
(a)如果使B气体的原子核激发后,马上抽去隔板,求扩散完成后气体的熵增加值.
(b)如果使B气体的原子核激发后,经过远大于激发态寿命的时间再抽去隔板,求气体的熵增加值.
参考答案:

2、试根据热力学第三定律证明,在T—>0时,一级相变两相平衡曲线的斜率 为零.
为零.
参考答案:
3、热力学第三定律要求遵从居里-外斯定律

的顺磁性固体,在足够低的某一温度发生相变,试加以证明.
第4题
糖透过.实验发现,糖水溶液的液面比容器内的水现.上升一个高度h,表明在同样温度下糖水溶液的压强p与水的压强p。之差为
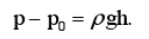
这一压强差称为渗透压、从理想溶液化学势的表达式可知,如果糖的水溶液与纯水具有相同的压强和温度,糖水溶液的化学势将低于纯水的化学势.因此水将从容器流入玻璃管,直到糖水的压强增为p,两相的化学势相等而达到平衡.平衡时有
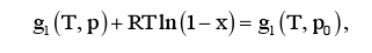
其中g1是纯水的摩尔吉布斯函数,x是糖水中糖的摩尔分数,
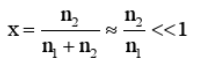
(n1,n2,分别是糖水中水和糖的物质的量).试据证明
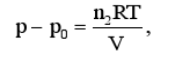
V是糖水溶液的体积.

第5题
承4.4题:
(a)试证明,在一定压强下溶剂沸点随溶质浓度的变化率为

其中L为纯溶剂的汽化热
(b)假设x<<1.试证明,溶液沸点升高与溶质在溶液中的浓度成正比,即
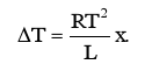
第6题
理想溶液中各组元的化学势为
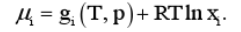
(a)假设溶质是非挥发性的.试证明,当溶液与溶剂的蒸气达到平衡时,相平衡条件为

其中g'是蒸气的摩尔吉布斯函数,g是纯溶剂的摩尔吉布斯函数,x是溶质在溶液中的摩尔分数.
(b)求证:在一定温度下,溶剂的饱和蒸气压随溶质浓度的变化率为
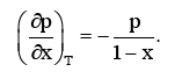
(c)将上式积分,得
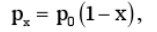
其中p0是该温度下纯溶剂的饱和蒸气压,pX是溶质浓度为x时的饱和蒸气压.上式表明,溶剂饱和蒸气压的降低与溶质的摩尔分数成正比,该公式称为拉乌定律,
第8题
A、2
B、1
C、1/2
D、0
第9题
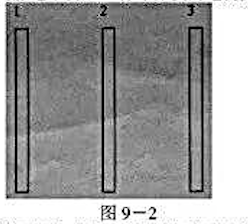
如图9-2所示,有3块平行放置的正方形大导体平板 1、2和3,每块板边长为L,相邻两板间距为d(d<0),将导体平板 1、2和3分别带电为q、2q和3q (q>0),求:
(1)各导体板的电荷分布。
(2)若将导体平板1和3接地,达到静电平衡后,各导体板的电荷分布。
第10题
如图9-1所示,一半径为R的导体球接地,在距导体球心为r处放置一个电量为q的点电荷。
(1)求达到静电平衡后,导体球带有的感应电荷的电量。
(2)若导体球不接地,求导体球的电位和点电荷q所受的力。



为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧