 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


某基元反应A(g)+ B(g)→P(g),设在298 K时的速率常数kp(298 K)=308 K时, .若A(g)和B(g)的原子半
某基元反应A(g)+ B(g)→P(g),设在298 K时的速率常数kp(298 K)=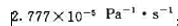 308 K时,
308 K时,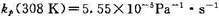 .若A(g)和B(g)的原子半径和摩尔质量分别为
.若A(g)和B(g)的原子半径和摩尔质量分别为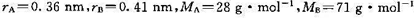 .试求在298 K时,(1)该反应的概率因子P;(2)反应的活化焓
.试求在298 K时,(1)该反应的概率因子P;(2)反应的活化焓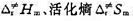 和活化Gibbs自由能
和活化Gibbs自由能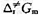 .
.
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


某基元反应A(g)+ B(g)→P(g),设在298 K时的速率常数kp(298 K)=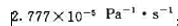 308 K时,
308 K时,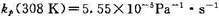 .若A(g)和B(g)的原子半径和摩尔质量分别为
.若A(g)和B(g)的原子半径和摩尔质量分别为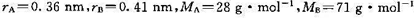 .试求在298 K时,(1)该反应的概率因子P;(2)反应的活化焓
.试求在298 K时,(1)该反应的概率因子P;(2)反应的活化焓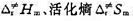 和活化Gibbs自由能
和活化Gibbs自由能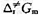 .
.
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“某基元反应A(g)+ B(g)→P(g),设在298 K时的…”相关的问题
更多“某基元反应A(g)+ B(g)→P(g),设在298 K时的…”相关的问题
第1题
已知乙炔气体的热分解是二级反应,发生反应的临界能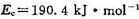 ,分子直径为 0.5 nm ,试计算:(1) 800 K.101.325 kPa时,单位时间、单位体积内的碰撞数;(2)上述反应条件下的速率常数;(3)上述反应条件下的初始反应速率。
,分子直径为 0.5 nm ,试计算:(1) 800 K.101.325 kPa时,单位时间、单位体积内的碰撞数;(2)上述反应条件下的速率常数;(3)上述反应条件下的初始反应速率。
请帮忙给出正确答案和分析,谢谢!
第2题
用波长为313 nm的单色光照射气态丙酮,发生下列分解反应:

若反应池的容量是0.059dm3,丙酮吸收入射光的分数为0.915,在反应过程中,得到下列数据:
反应温度840 K
照射时间t=7.0 h
起始压力102. 16 kPa
入射能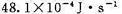
终了压力104.42kPa
计算此反应的量子效率。
请帮忙给出正确答案和分析,谢谢!
第3题
有一酶催化反应CO2(aq)+H2O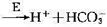 ; 设H2O大大过量,溶液的pH=7. 1,温度为0. 5℃,酶的初始浓度
; 设H2O大大过量,溶液的pH=7. 1,温度为0. 5℃,酶的初始浓度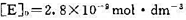 。实验测得反应初速率ro随CO2(g)的初始浓度[CO2]。的变化如下所示:
。实验测得反应初速率ro随CO2(g)的初始浓度[CO2]。的变化如下所示:

试求:(1) Michaelis常数Km及最大反应速率rm; (2)中间配合物的速率常数k2;(3)从速率方程如何理解Km是反应速率为最大反应速率rm的一半时底物的浓度,即r=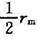 时,KM= [S].
时,KM= [S].
请帮忙给出正确答案和分析,谢谢!


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧