 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在锌电极上析出氢气的Tafel公式为在298K时,用Zn(s)作阴极,惰性物质作阳极,电解浓度为0.1mol·kg
在锌电极上析出氢气的Tafel公式为
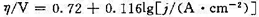
在298K时,用Zn(s)作阴极,惰性物质作阳极,电解浓度为0.1mol·kg-1的ZnSO4溶液,设溶液pH值为7.0,若要使H2(g)不和锌同时析出,应控制什么条件?
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在锌电极上析出氢气的Tafel公式为
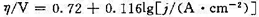
在298K时,用Zn(s)作阴极,惰性物质作阳极,电解浓度为0.1mol·kg-1的ZnSO4溶液,设溶液pH值为7.0,若要使H2(g)不和锌同时析出,应控制什么条件?
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“在锌电极上析出氢气的Tafel公式为在298K时,用Zn(s…”相关的问题
更多“在锌电极上析出氢气的Tafel公式为在298K时,用Zn(s…”相关的问题
第1题
氯碱工业用铁网为阴极,石壘棒为阳极,电解含NaCl的质量分数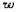 (NaCl)= 0.25的溶液来获得Cl2(g)和NaOH溶液。NaCl溶液不断地加到阳极区,然后经过隔膜进人阴极区。若某电解槽内阻为8×10-4Ω,外加电压为4.5V,电流强度为2000A.每小时从阴极区流出溶液为27.46kg,其中
(NaCl)= 0.25的溶液来获得Cl2(g)和NaOH溶液。NaCl溶液不断地加到阳极区,然后经过隔膜进人阴极区。若某电解槽内阻为8×10-4Ω,外加电压为4.5V,电流强度为2000A.每小时从阴极区流出溶液为27.46kg,其中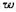 (NaOH) =0.10,
(NaOH) =0.10,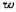 (NaCl)=0.13。已知下述电池的电动势为2.3 V:
(NaCl)=0.13。已知下述电池的电动势为2.3 V:
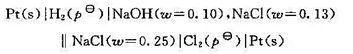
试求:(1)该生产过程的电流效率;(2)该生产过程的能量效率(即生产一定量产品时,理论上所需的电能与实际消耗的电能之比);(3)该电解池中用于克服内阻及用于克服极化的电势降各为多少。
第2题
有下列几种:
酸性条件
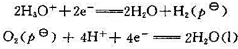
碱性条件
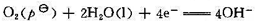
所谓金属腐蚀是指金属表面附近能形成离子的活度至少为10-6。现有如下6种金属:Au、Ag、Cu,Fe.Pb和AI。试问哪些金属在下列pH值条件下会被腐蚀?
(1)强酸性溶液pH=1;
(2)强碱性溶液pH= 14;
(3)微酸性溶液pH= 6;
(4)微碱性溶液pH=8。
所需的标准电极电势值白己查阅,设所有活度因子均为1.
第3题
在298 K和标准压力下,以Pt为阴极,C(石墨)为阳极,电解含CdCl2(0. 01 mol·kg-1)和CuCl2(0.02 mol·kg-1)的水溶液。若电解过程中超电势可忽略不计,试问(设活度因子均为1):(1)何种金属先在阴极析出? (2) 第二种金属析出时,至少须加多少电压? (3) 当第二种金属析出时,第一种金属离子在溶液中的浓度?(4)事实上O2(g)在石墨上是有超电势的,若设超电势为0.85V,则阳极上首先应发生什么反应?
第4题
工业上目前电解食盐水制造NaOH的反应为
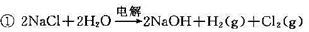
有人提出改进方案,改造电解池的结构,使电解食盐水的总反应为
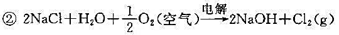
(1)从两种电池总反应分别写出阴极和阳极反应;
(2)计算在298 K时,两种反应的理论分解电压各为多少。设活度均为1,溶液pH=14;
(3)计算改进方案在理论上可节约多少电能(用百分数表示)。
第5题
在298K时使下述电解池发生电解作用:
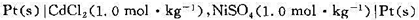
问当外加电压逐渐增加时,两电极上首先分别发生什么反应?这时外加电压至少为多少? (设活度因子均为1,超电势可忽略。)
第6题
在298 K和标准压力时,电解含有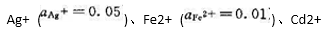
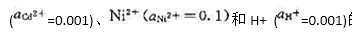 的混合溶液,并设
的混合溶液,并设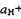 不随电解的进行而变化,又已知H2(g)在Ag、Ni、Fe和Cd上的超电势分别为0.20 V、 0.24 V、0.18 V和0.30 V.当外加电压从零开始逐渐增加时,试用计算说明在阴极上析出物质的顺序。
不随电解的进行而变化,又已知H2(g)在Ag、Ni、Fe和Cd上的超电势分别为0.20 V、 0.24 V、0.18 V和0.30 V.当外加电压从零开始逐渐增加时,试用计算说明在阴极上析出物质的顺序。
第7题
在298K和标准压力下,用镀铂黑的铂电极电解aH+=1.0的水溶液,当所用的电流密度j=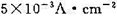 时,计算使电解能顺利进行的最小分解电压。已知
时,计算使电解能顺利进行的最小分解电压。已知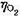 =0.487V,
=0.487V,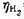 ≈0,忽略电阻引起的电位降,H2O(I)的标准摩尔生成Gibbs自由能
≈0,忽略电阻引起的电位降,H2O(I)的标准摩尔生成Gibbs自由能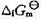 =-237.129kJ·mol-1.
=-237.129kJ·mol-1.
第8题
第9题
298 K时,反应 的恒容热效应Qv=- 252.79kJ·mol-1.在298 K、
的恒容热效应Qv=- 252.79kJ·mol-1.在298 K、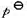 下,将上述反应体系构成一可道原电池,则其电动势的温度系数为
下,将上述反应体系构成一可道原电池,则其电动势的温度系数为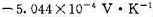 。求Ag(s) |Ag2O(s)|OH-电极的
。求Ag(s) |Ag2O(s)|OH-电极的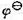 。已知298 K时水的离子积
。已知298 K时水的离子积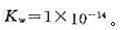 。
。
第10题
试由下列数据求出298 K下,Cu(s)、CuI(s)、HI(aq)及H2( )体系达平衡时HI的浓度。假设HI在水溶液中完全解离,其平均活度系数
)体系达平衡时HI的浓度。假设HI在水溶液中完全解离,其平均活度系数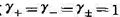 ;CuI的溶度积为
;CuI的溶度积为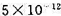 ,
,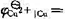 0.337 V;当Cu2+ 、Cu+与金属铜达成平衡时
0.337 V;当Cu2+ 、Cu+与金属铜达成平衡时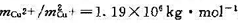 .设活度因子均为1.
.设活度因子均为1.


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧