 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
试设计一个电池,使其中进行下述反应(1)写出电池的表达式;(2)计算上述电池反应在298 K、反应进
试设计一个电池,使其中进行下述反应
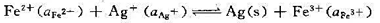
(1)写出电池的表达式;(2)计算上述电池反应在298 K、反应进度为1 mol时的平衡常数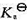 ;(3)若将过量磨细的银粉加到浓度为0.05mol·kg-1的Fe(NO3)3,溶液中,求当反应达平衡后,Ag+的浓度为多少(设活度因子均等于1)?
;(3)若将过量磨细的银粉加到浓度为0.05mol·kg-1的Fe(NO3)3,溶液中,求当反应达平衡后,Ag+的浓度为多少(设活度因子均等于1)?
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
试设计一个电池,使其中进行下述反应
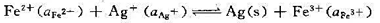
(1)写出电池的表达式;(2)计算上述电池反应在298 K、反应进度为1 mol时的平衡常数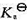 ;(3)若将过量磨细的银粉加到浓度为0.05mol·kg-1的Fe(NO3)3,溶液中,求当反应达平衡后,Ag+的浓度为多少(设活度因子均等于1)?
;(3)若将过量磨细的银粉加到浓度为0.05mol·kg-1的Fe(NO3)3,溶液中,求当反应达平衡后,Ag+的浓度为多少(设活度因子均等于1)?
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“试设计一个电池,使其中进行下述反应(1)写出电池的表达式;(…”相关的问题
更多“试设计一个电池,使其中进行下述反应(1)写出电池的表达式;(…”相关的问题
第1题
298 K时,下述电池的E为1.228 V:
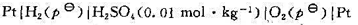
已知H2O(1)的标准摩尔生成焓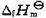 (H2O,l)=- 285.83 kJ·mol-1,试求:(1)该电池的温度系数;(2)该电池在273 K时的电动势。设反应焓在该温度区间内为常数。
(H2O,l)=- 285.83 kJ·mol-1,试求:(1)该电池的温度系数;(2)该电池在273 K时的电动势。设反应焓在该温度区间内为常数。
请帮忙给出正确答案和分析,谢谢!
第3题
298 K时,已知如下电池的标准电动势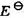 =0.2680V:
=0.2680V:
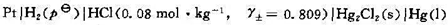
(1)写出电极反应和电池反应;(2)计算该电池的电动势;(3)计算甘汞电极的标准电极电势。
请帮忙给出正确答案和分析,谢谢!
第4题
电池Zn |ZnCl2( 0. 05mol·kg-1) |AgCI(s) |Ag(s)的电动势与温度的关系为E/V=1.015一4.92×10-4(T/K-298)。试计算在298K,当电池有2mol电子的电荷量输出时,电池反应的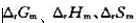 和此过程的可逆热效应QR.
和此过程的可逆热效应QR.
请帮忙给出正确答案和分析,谢谢!


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧