题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知298 K时,Ba2+aq和SO·aq的标准摩尔生成焓为-537.65 kJ·mol-1和-907.5 kJ·mol-1,反应:BaCl2·aq + Na2SO4·aq == BaSO4(s) + 2NaCl·aq的标准摩尔焓变是-20.08 kJ·mol-1,计算得BaSO4(s)的标准摩尔生成焓为()。 (aq代表大量的水)
A.1465.23 kJ·mol-1
B.-1465.23 kJ·mol-1
C.1425.07 kJ·mol-1
D.-1425.07 kJ·mol-1
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案


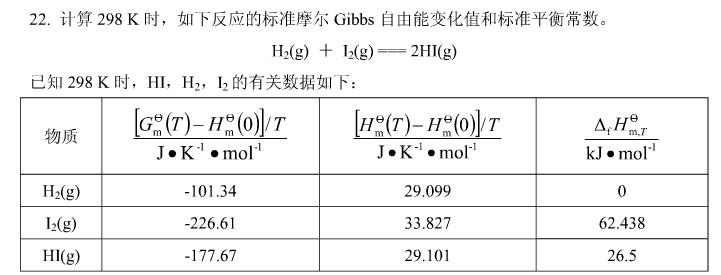

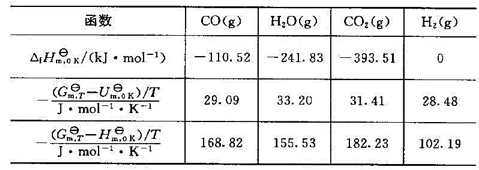

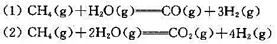
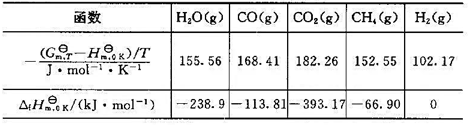
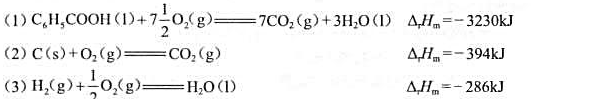 求C6H5COOH(1)的标准生成热ΔHƟm。
求C6H5COOH(1)的标准生成热ΔHƟm。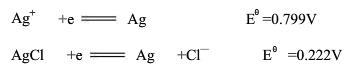
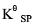 。
。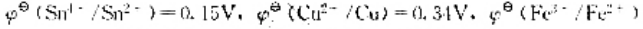
 ,判断下列各组物质在标准状态下能共存的是()。
,判断下列各组物质在标准状态下能共存的是()。
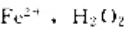


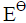 =0.2680V:
=0.2680V: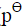 )|HCl(0.08mol·kg-1, γ±=0.809)|Hg2Cl2(s)|Hg(l)
)|HCl(0.08mol·kg-1, γ±=0.809)|Hg2Cl2(s)|Hg(l)