 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
丙酮和碘的反应为:此反应能被H+催化,其催化常数k0=4.48X10-4mol-1·dm3
丙酮和碘的反应为:
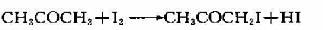
此反应能被H+催化,其催化常数k0=4.48X10-4mol-1·dm3·s-1,试计算当[H+]=0.05mol·dm3和[H+]==0.10mol·dm3时此反应的速军常数:
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
丙酮和碘的反应为:
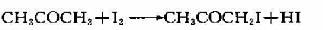
此反应能被H+催化,其催化常数k0=4.48X10-4mol-1·dm3·s-1,试计算当[H+]=0.05mol·dm3和[H+]==0.10mol·dm3时此反应的速军常数:
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“丙酮和碘的反应为:此反应能被H+催化,其催化常数k0=4.4…”相关的问题
更多“丙酮和碘的反应为:此反应能被H+催化,其催化常数k0=4.4…”相关的问题
第1题
通常ΔvapHm是与温度有关的,当ΔvapHm=f(T)时,试推导lnp=f(T)的关系式.
(1)假设ΔvapHm=a+bT;
(2)假设ΔvapHm=a+bT+cT2;
(3)已知Hg的饱和蒸气压可以用下列公式表示:
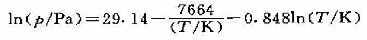
试计算Hg在25℃时汽化热为若干?
第2题
Si-Ge系统的熔融液体由高温缓慢冷却时,取得下列数据:

(1)试画出此系统的相图,标明每个区域和每条线的含义;
(2)任何组成的Si-Ge熔融液冷却时所形成的固相有何特征.
第3题
在25℃时,电池
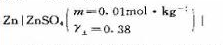
|PbSO4-Pb(s)的电动势E=0.5477V.(1)已知φθ(Zn2+|Zn)=-0.763V,求φθ(PbSO4|Pb(2)已知25℃时PbSO4的K =1.58×10-8,求φθ(Pb2+|Pb);(3)当ZuSO4的m=0.050mol·kg-1时,E=0.5230V,求此浓度下ZnSO4的y
=1.58×10-8,求φθ(Pb2+|Pb);(3)当ZuSO4的m=0.050mol·kg-1时,E=0.5230V,求此浓度下ZnSO4的y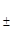 .
.
第4题
在25℃时,有电池:
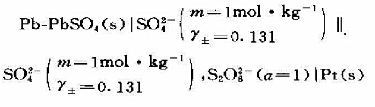
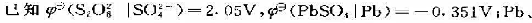
PbSO4、SO42、SO42的标准熵值分别为64.89、147.28、146.14、17.15J·K·mol-1.试计算该温度下,电池以端电压2.0V不可逆放电时的热效应.
第6题
比电极,用φθ(玻)=0.3690V的玻璃电极作指示电极,分别计算当加入0.00、9.00、9.90、9.99、10.00、10.01、10.10、11.00、20.00cm3碱液后,玻璃电极的电势φ(玻)为多少,并以(玻)为纵坐标,以滴定液体积为横坐标作出滴定曲线.假定滴定中系统体积变化可忽略.
第7题
已知25℃时,HgO(s)的ΔrG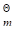 =-58.5kJ·mol-1,电池(Pt)H2(pθ)|KOH(aq)|HgO(s)-Hg(l)的Eθ=0.926V,水的离子积K
=-58.5kJ·mol-1,电池(Pt)H2(pθ)|KOH(aq)|HgO(s)-Hg(l)的Eθ=0.926V,水的离子积K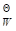 =10-14.求OH-的标准摩尔生成吉布斯自由能ΔrG
=10-14.求OH-的标准摩尔生成吉布斯自由能ΔrG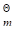 ;
;
第8题
时AgCI的Kθ=1.69X10-10,求φθ(Ag-1Ag);

(3) 在25℃时,电池Ag-AgCl|HCl|Hg2Cl2-Hg的E=0.0456V,求φθ(Hg2Cl2|Hg).
第9题
试设计一个电池,使其中进行下述反应:

(1)写出电池表示式;
(2)计算25℃时,上述电池反应的Kθ;
(3)若将过量的银粉加到浓度为0.05mol·kg-1的Fe(NO3)3溶液中,求反应达平衡后Ag+的浓度为多少?(设活度系数均为1).已知φθ(Fe3+|Fe2+)=0.771V,φθ(Ag|Ag+)=0.7991V.
第10题
在25℃时,电池:
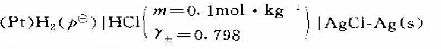
的电动势E=0.3522V.试求:
(1)反应H2(g)+2AgCl(s)=2Ag(s)+2HCl(0.1mol·kg-1)的Kθ;
(2)金属银在Y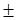 =0.809的1mol·kg-1HCl中所能产生的H2的平衡分压力.
=0.809的1mol·kg-1HCl中所能产生的H2的平衡分压力.


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧