 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
0.25mol•L-1NaH2PO4溶液100mL和0.35mol•L-1NaH2PO4溶液50mL混合后,溶液的pH值为多少?若向溶液中加入0.10mol•L-1NaOH溶液50mL,溶液的pH值为多少?(H3PO4的Ka1=6.9x10^-3,Ka2=6.3x10^-8)。
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“0.25mol•L-1NaH2PO4溶液100mL和0.35…”相关的问题
更多“0.25mol•L-1NaH2PO4溶液100mL和0.35…”相关的问题
第2题
第3题
第4题
用0.100mol?L-1的NaOH溶液滴定0.100mol?L-1二元弱酸H2B。已知:pH=0.74时,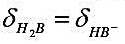 ;pH==6.50时,
;pH==6.50时,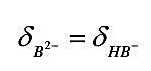 ;求该二元弱酸H2B的Ka1与Ka2。
;求该二元弱酸H2B的Ka1与Ka2。
请帮忙给出正确答案和分析,谢谢!


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧